上海第二军医大学长海医院风湿免疫科 中国上海 200433
【摘要】目的:旨在评价接受了TNF-α拮抗剂治疗的中国汉族人群强直性脊柱炎患者的副反应,为生物制剂的临床治疗提供参考依据。方法:本研究纳入在我科接受了TNF-α拮抗剂治疗的369例中国汉族人群强直性脊柱炎,未完全跟踪随访给药1011次。所有患者均评估了用药后(2h)出现的副反应,对其中126人长期用药患者进行了(8周、12周、52周、104周)的随访。其中用药后(2h)的轻度副反应:头痛、皮疹、眩晕、恶心;中度副反应:发热、皮肤过敏、心悸、呼吸困难、腹痛、血压变化;重度副反应:寒颤伴高热、头痛伴视物模糊、心悸伴血压升高。长期用药的副反应可能包括:肺炎、尿路感染、中耳炎、反应迟钝、结核复发。结果:所有接受1011次TNF-α拮抗剂治疗的369例AS患者:652次(64.5%)重组人Ⅱ型肿瘤坏死因子受体-抗体融合蛋白(益赛普,rhTNFR-Fc)、316次(31.3%)英夫利西单抗(类克,Remicade)、21次(2%)依那西普(恩利,Enbrel)、22次(2.2%)阿达木单抗(修美乐,adalimumab)。随访用药后(2h)共计30次发生副反应:益赛普17次(2.6%)、类克12次(3.7%)、恩利0次(0%)、修美乐1次(4.5%)。其中轻度21次(益赛普12次,类克9次),中度5次(益赛普3次,类克1次,修美乐1次),重度4次(益赛普2次,类克2次),类克和益赛普引起短期(注射2h后)副反应相当(3.7%vs2.6%,P=0.31>0.05)。126例(益赛普69例,类克57例)患者分别依次进行了第8周、12周、52周、104周的随访,共计39例发生副反应:益赛普20例(51.3%)、类克19例(48.7%)。感染性疾病37例(94.9%)、神经系统病变1例(2.6%)、结核复发1例(2.6%),长期应用类克和益赛普(51.3%vs48.7%,P=0.69>0.05)副反应相当,以感染性炎症发生为主,需要注意神经系统病变和结核复发可能。结论:中国汉族人群强直性脊柱炎患者在接受TNF-α拮抗剂治疗应注意上述副反应的发生,接受类克和益赛普治疗的患者用药后2h内和长期(≥2年)治疗的副反应发生相当。
【关键词】:脊柱炎,强直性;TNF-α拮抗剂;治疗结果;安全性
Abstract Objective To evaluate TNF-αblocker treatment of Chinese Han population patients with ankylosing spondylitis,aim to support a clinal experience to Chinese doctor.Methods This study enrolled 369 Chinese Han population patients with ankylosing spondylitis,which received TNF-αblocker treatment in our Department.In total,administrate 1011 times.All of them were evaluated on adverse events after injected 2 hours later,126 of them received long-term TNF-αblocker drugs,follow-up visit at week 8、12、52、104。Mild immediate adverse events include:headache,rash,dizziness,nausea,moderate:fever,urticaria,palpitation, abdominalgia,dyspnea,blood pressure variation.severe:fever with chills,dyspnea with blur, palpitation with acute blood pressure evaluation.Long-term drugs used may occur:pneumonia,urinary tract infection, tympanitis,unresponsive,tuberculosis relapse. Results All 369 patients were administrated 1011 times, 652(64.5%)rhTNFR-Fc, 316(31.3%)Remicade , 21(2%)Enbrel , 22(2.2%)adalimumab. adverse events after injected 2 hours later: 17(2.6%)rhTNFR-Fc, 12(3.7%)Remicade, 0(0%)Enbrel、1(4.5%)adalimumab.Mild 21 times(12 rhTNFR-Fc, 9 Remicade); moderate 5 times (3 rhTNFR-Fc, 1 Remicade,1 adalimumab); severe 4 times(2 rhTNFR-Fc, 2 Remicade). Outcome were comparable with rhTNFR-Fc and Remicade in immediate reaction(3.7%vs2.6%,P=0.31>0.05).Long-term used frugs of 126( 69 rhTNFR-Fc, 57 Remicade) patients, follow-up at week 8、12、52、104,39 patients occure: 20(51.3%)rhTNFR-Fc, 19(48.7%)Remicade . 37 Infectious diseases(94.9%), 1 neurological disease(2.6%), 1 tuberculosis relapse(2.6%), Outcome were comparable with rhTNFR-Fc and Remicade in long-term used, infectious diseases prior to other diseases,need monitoring neurological disease and tuberculosis relapse.Conclusion It is shows that TNF-αblocker treatment of Chinese Han population patients with ankylosing spondylitis need focusing on above adverse events,occurrence were comparable with rhTNFR-Fc and Remicade in immediate reaction or long-term used.
Key words:Spondylitis,ankylosing; TNF-α Blocker;Treatment outcome ;Safety
强直性脊柱炎(ankylosing spondylitis,AS)是一种男性青壮年多发累及中轴关节为主的自身免疫性疾病,在疾病的进展中,以骨破坏与骨形成交替进行为特征,给社会和家庭造成了沉重的社会和经济负担[1-2]。当前随着生物制剂的出现,对于一些应用传统药物治疗无效的风湿病患者,从而更多的选择肿瘤坏死因子(TNF-α)拮抗剂治疗。TNF-α拮抗剂能够靶向拮抗炎症因子的释放,迅速缓解病情,甚至能够阻止其影像学进展[3-4]。任何药物的安全性使用都必须建立在了解其副反应的基础上。目前为止,TNF-α拮抗剂已经被证实在治疗中国汉族人群的AS患者起效迅速,疗效确切[5-6],但在药物应用的安全性上,还未有大规模的研究报道。TNF-α拮抗剂在中国汉族人群AS患者的首次用药和长期应用发生的副反应还仍不十分清楚。因此本研究随访总结了我科369例中国汉族人群AS患者应用1011次TNF-α拮抗剂治疗发生的副反应,并监测我科AS数据库中126例长期(≥2年)应用TNF-α拮抗剂的副反应,发现TNF-α拮抗剂治疗中国汉族人群AS患者副反应发生较少,长期使用应注意感染性炎症的发生。
1 资料和方法
1.1 病例选择
本研究纳入从2008年6月至2011年3月在我科门诊和住院部接受了TNF-α拮抗剂治疗的1011例中国汉族人群类风湿关节炎和强直性脊柱炎的患者,其中男性348例,女性21例,平均年龄27.6岁,AS所有患者均符合1984年修订的AS纽约分类标准,在纳入研究时已签署知情同意书。
1.2 治疗方法
TNF-α拮抗剂包括:英夫利西单抗(类克,Remicade)静脉给药,重组人Ⅱ型肿瘤坏死因子受体-抗体融合蛋白(益赛普,rhTNFR-Fc)、依那西普(恩利,Enbrel)、阿达木单抗(修美乐,adalimumab)均为皮下注射。所有患者在首次给药2h内由专职医生或者医嘱执行护士评价副反应发生,长期应用TNF-α拮抗剂治疗的患者由专职医生跟踪随访,给药前排除活动性结核;慢性肝炎;急慢性感染;全身各脏器影响功能病变者。治疗方案:重组人Ⅱ型肿瘤坏死因子受体-抗体融合蛋白(2次/周),英夫利西单抗(0,2,6,8周,以后每8周一次),阿达木单抗(1次/2周),依那西普(1次/1周)。英夫利西单抗(200mg/次,静脉注射),给药时间约2-3h左右,其他的TNF-α拮抗剂均为皮下注射,注射时评估2h内的副反应。专职医生筛选出AS数据库中长期单一应用TNF-α拮抗剂的126例患者进行了(8周、12周、52周、104周)的副反应随访,排除合并应用非甾体类药物和传统的抗风湿改善病情药物(DMARDs)的患者,签署知情同意书承诺在随访期间不擅自更换药物使用和加用其他类药物。
1.3 首次用药副反应观察
首次用药期间由专职医生或医嘱执行护士进行副反应评估分级。轻度:头痛、皮疹、眩晕、皮肤瘙痒、恶心;中度:发热、皮肤过敏、心悸、呼吸困难、胸痛、腹痛、血压升高;重度:寒颤伴高热、头痛伴视物模糊、心悸伴血压升高。
1.4 长期用药副反应观察
长期用药的副反应由我科AS数据库的专职医生,在第8周、12周、52周、104周用药前进行副反应的观察评估包括:感染性炎症:肺炎、尿路感染、中耳炎、结核复发;神经系统病变:反应迟钝(患者自述)。
1.5 统计学分析
数据统计结果采用百分比表示(%),Fisher确切检验P值分析比较两种TNF-α拮抗剂(益赛普vs类克)副反应关联的统计学意义,P<0.05具有统计学意义。恩利(21例)和修美乐(22例)病例数较少,仅作简单报告,不做任何统计学分析。
2结 果
369例中国汉族人群强直性脊柱炎患者接受共计1011次TNF-α拮抗剂治疗:652次(64.5%)重组人Ⅱ型肿瘤坏死因子受体-抗体融合蛋白(益赛普,rhTNFR-Fc)、316次(31.3%)英夫利西单抗(类克,Remicade)、21次(2%)依那西普(恩利,Enbrel)、22次(2.2%)阿达木单抗(修美乐,adalimumab)(图表1)。
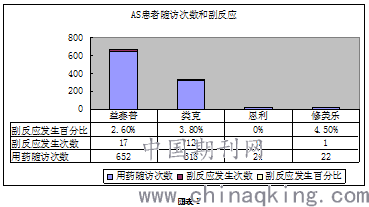
用药后(2h)随访共计30/1011(3%)发生副反应:益赛普17/652(2.6%)、类克12/316(3.8%)、恩利0/22(0%)、修美乐1/22(4.5%)。其中轻度21/30(70%)(益赛普12次,类克9次),中度5/30(16.7%)(益赛普3次,类克1次,修美乐1次),重度4/30(13.3%)(益赛普2次,类克2次),发生轻度副反应予以(类克)调慢静脉滴注速度或者推注葡萄糖酸钙,中重度以上副反应患者予以地塞米松5mg静推以及吸氧、降压等对症支持治疗,症状仍未缓解者转诊急诊监护病房实行72h监护治疗,所有发生短期副反应的AS患者经治疗2h-72h后,副反应消失,症状好转。
随访126例长期用药患者(益赛普69例,类克57例),由专职医生依次在第8周、12周、52周、104周进行随访,共计39/126(31%)发生副反应:益赛普20/39(51.3%)、类克19/39(48.7%)。感染性炎症37/39例(94.8%)、神经系统病变1/39例(2.6%)、结核复发1/39(2.6%)(图表2)。所有长期应用TNF-α拮抗剂治疗的AS患者发生副反应时,全部暂时予以停用TNF-α拮抗剂治疗,感染性炎症予抗生素正规疗程抗感染治疗,由风湿科医生和呼吸科、泌尿外科、耳鼻喉科、放射科医生重新评估后,重新予以TNF-α拮抗剂治疗;神经系统病变(反应迟钝)患者予以停用TNF-α拮抗剂治疗,反应迟钝症状较前明显好转。结核复发患者予以转诊结核病医院进行正规抗结核治疗,目前仍在随访中。
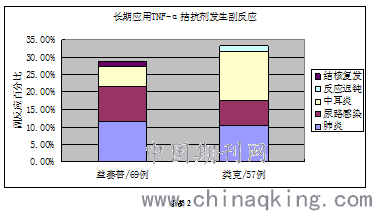
TNF-α拮抗剂用药后(2h)随访发生副反应:益赛普17/652(2.6%)、类克12/316(3.7%),类克和益赛普在用药短期内发生副反应相当(P>0.05)。恩利(21次)和修美乐(22次)用药次数较少,在此暂时不做统计学分析,仅做简单报告。
126例(益赛普69例,类克57例)AS患者由专职医生依次进行了第8周、12周、52周、104周的随访,共计39例发生副反应:益赛普20例(51.3%)、类克19例(48.7%),单一长期使用类克或益赛普药物的患者发生副反应机会相当(P>0.05)。
3讨 论
TNF-α拮抗剂是一种靶向拮抗AS炎症因子释放,能够有效快速的阻滞病情进展,防止骨质破坏的生物制剂[7-8]。由于其确切的疗效,在临床中得到了极为广泛的应用。然而随着TNF-α拮抗剂在AS或RA等风湿病患者中药物使用的数量和时间增加,有研究报道发现一些常见和罕见的副反应。这些副反应虽然发生率很少,但是有些却很严重[9-11],而在一些长期使用药物的患者中间,我们也发现了一些说明书上提及或者未提及的副反应,这些副反应的发生提示我们医生应该在有监测条件的情况下使用TNF-α拮抗剂。
本研究建立了由专职医生或护士进行的标准副反应评估体系,短期监测首次应用TNF-α拮抗剂(皮下、静滴)治疗中或治疗结束2h内发生的一切副反应,从我科建立的AS数据库筛选出单纯应用TNF-α拮抗剂的患者进行长期的跟踪随访,数据库专职医生监测药物使用的长期累积副反应。本设计研究方案旨在为临床医生提供中国人群的AS患者使用TNF-α拮抗剂治疗在短期和长期应用中可能会发生的副反应,以便建立有效的预防和干预体系,更明确的监测这类副反应的发生,为药物的更好使用提供初步的理论依据。
本研究发现在中国AS患者中使用中:用药后(2h)随访共计30/1011(3%)发生副反应:益赛普17/652(2.6%)、类克12/316(3.7%)、恩利0/22(0%)、修美乐1/22(4.5%)。上述结果与国外人群接收TNF-α拮抗剂治疗副反应发生率约为3.7%报道类似[12],其中类克可能由于其鼠源化的成分导致排斥反应的发生率更高,从而使得其副反应的发生率相对较高。我们监测长期使用TNF-α拮抗剂的126例(益赛普69例,类克57例)AS患者,共计39/126(31%)发生副反应,益赛普20/69(51.3%)、类克19/57(48.7%)。感染性炎症37/39(94.8%)、神经系统病变1/39(2.6%)、结核复发1/39(2.6%),其中感染性炎症包括:肺炎14/39(35.9%)、尿路感染11/39(28.2%)、中耳炎12/39(30.8%)。上述结果和国外人群报道长期接受TNF-α拮抗剂的RA和AS患者约24%左右人群出现感染的发生率相似[13-14]。然而其中尿路感染的发生时间大多数在54周的用药随访期间,而本次研究纳入人群以青年男性为主,发生尿路感染的患病率较低,所以尿路感染发生原因可能是由于TNF-α拮抗剂长期使用造成的,也可能为疾病本身造成。由于我国是一个结核感染严重的国家,其中有一例出现了结核复发,经过专科医院正规抗结核治疗后好转,目前为止仍在随访中。其中有1例患者的职业是摄影师,工作中需要精准快速的反应,但在用药后第8周后就自述工作时不够集中,反应迟钝。我们在将其转诊至经神经科医生评估后,确认患者自身否认合并存在其他神经精神系统实质性病变,予以停止TNF-α拮抗剂(类克)的治疗,停药2周后症状好转,可能由于TNF-α拮抗剂导致神经系统传导障碍或者大脑皮质层中枢的未知病变,虽然在精神系统的副反应中有周围神经炎、多发性硬化、视神经炎、急性横贯性脊髓炎等中枢神经性病变的报道[15],但国外研究尚未有造成患者反应迟钝的副反应报道。因此上述研究结果表明,在长期使用TNF-α拮抗剂的AS患者中,医生应该监测其感染性炎症的发生,注意神经系统的病变,重视结核的感染。
TNF-α拮抗剂在中国人群AS患者中使用安全可靠,但要注意首次用药和长期用药的副反应的发生。风湿科医生应该定期监测和随访药物使用的副反应,尤其是说明书和文献未有报道的潜在副反应,通过随访及时了解患者病情变化,根据病情变化调整治疗方案。首次应用TNF-α拮抗剂的AS患者,应该在医生和护士的监测和评估下使用药物,尽可能避免在未有监测和及时治疗的条件下应用,长期使用的患者应加强与医生的沟通,定期随访,及时调整治疗方案。
参考文献
[1]Dillon CF, Hirsch R.The United States National Health and Nutrition Examination Survey and the Epidemiology of Ankylosing Spondylitis in the United States. Am J Med Sci,2011,23
[2]Bakland G,Gran JT, Becker-Merok A et al.Work disability in patients with ankylosing spondylitis in norway. J Rheumatol,2011,38:479-84
[3]Braun J, van der Horst-Bruinsma IE, Huang F et al.Clinical efficacy and safety of etanercept versus sulfasalazine in ankylosing spondylitis patients: A randomized, double-blind study (ASCEND Trial). Arthritis Rheum,2011,10
[4]Martín-Mola E,Sieper J, Leirisalo-Repo M et al.Sustained efficacy and safety, including patient-reported outcomes, with etanercept treatment over 5 years in patients with ankylosing spondylitis.Clin Exp Rheumatol,2010,28:238-45
[5]黄烽,邓小虎,张亚美等.重组人Ⅱ型肿瘤坏死因子受体-抗体融合蛋白治疗强直性脊柱炎的多中心双盲随机对照临床研究.中华风湿病学杂志,2008,12:314-320
[6]黄烽,张洁,黄建林等. 依那西普治疗强直性脊柱炎的多中心、随机、双盲、安慰剂对照临床研究. 中华内科杂志,2010,9:741-745
[7]Rudwaleit M. Effects of low-dose infliximab on spinal inflammation on magnetic resonance imaging in ankylosing spondylitis. J Rheumatol,2010,37:1553-5
[8]Maksymowych WP,Salonen D,Inman RD et al.Low-dose infliximab (3 mg/kg) significantly reduces spinal inflammation on magnetic resonance imaging in patients with ankylosing spondylitis: a randomized placebo-controlled study. J Rheumatol.,2010,37:1728-34
[9]Nagy G, Lukács K, Sziray A et al. Adverse events during biological therapy - focusing on dermatological side-effects. Orv Hetil,2011,152:212-220
[10]Fouache D, Goëb V, Massy-Guillemant N et al. Paradoxical adverse events of anti-tumour necrosis factor therapy for spondyloarthropathies: a retrospective study. Rheumatology (Oxford),2009,48:761-4
[11]Gerloni V, Pontikaki I, Gattinara M et al. Focus on adverse events of tumour necrosis factor alpha blockade in juvenile idiopathic arthritis in an open monocentric long-term prospective study of 163 patients. Ann Rheum Dis,2008,67:1145-52
[12]de Moraes JC, Aikawa NE, Ribeiro AC et al. Immediate complications of 3,555 injections of anti-TNFα. Rev Bras Reumatol,2010,50:165-75
[13]Dixon WG, Watson K, Lunt M et al. Rates of serious infection, including site-specific and bacterial intracellular infection, in rheumatoid arthritis patients receiving anti-tumor necrosis factor therapy: results from the British Society for Rheumatology Biologics Register. Arthritis Rheum,2006,54:2368-76
[14]Levälampi T, Korpela M, Vuolteenaho K et al nfliximab treatment in patients with rheumatoid arthritis and spondyloarthropathies in one rheumatological center: two years' drug survival.Rheumatol Int,2010 ,30:1611-20
[15]Tristano AG. Neurological adverse events associated with anti-tumor necrosis factor alpha treatment. J Neurol,2010,257:1421-31
论文作者:童强 徐霞 孔瑞娜 庞亚飞 吉连梅 张菊 张兰玲 赵东宝 蔡
论文发表刊物:《临床医学教育》2018年4期
论文发表时间:2018/5/11
标签:拮抗剂论文; 副反应论文; 患者论文; 发生论文; 汉族论文; 医生论文; 中国论文; 《临床医学教育》2018年4期论文;
